
Da quanto si può notare non sono tutti ordinati secondo lo stesso numero quantico n. In chimica, in particolare in chimica quantistica, un orbitale molecolare è la distribuzione spaziale degli elettroni in una molecola. Introdotto da Friedrich Hund e Robert S. Per stabilire in quali orbitali atomici si accomodano gli elettroni si deve partire dal principio di esclusione di Pauli, dalla regola di Hund e dal diagramma delle energie.
Secondo il principio di Pauli in un atomo non vi possono essere due elettroni aventi gli stessi numeri quantici, ovvero in un livello energetico vi possono essere al massimo due elettroni e, se ve ne sono due, essi hanno spin opposti. Ordine di Riempimento degli Orbitali e Configurazione Elettronica degli Elementi Esistono delle specifiche regole di riempimento per sistemare gli elettroni nei rispettivi orbitali, e quindi.
L’ordine preciso degli orbitali dipende dal numero di elettroni presenti nell’atomo, e ce ne occuperemo nel prossimo paragrafo. Tali regioni furono chiamate orbitali. Con il termine configurazione elettronica di un elemento si intende la descrizione della disposizione degli elettroni nei suoi orbitali.
Quindi in un orbitale ci possono essere al massimo due elettroni. Se attorno a un atomo ci sono più di due elettroni, questi si trovano per forza in orbitali diversi. Esistono infatti molti tipi di orbitali, che vengono riempiti dagli elettroni seguendo un ordine particolare. I primi orbitali hanno queste forme strane.
Tali orbitali vanno riempiti rispettando la regola di Hund. Per prima cosa dovete considerare il numero degli elettroni presenti negli orbitali molecolari di. Questi orbitali sono simili alla forma orbitale p, ma con più ‘petali’ come un quadrifoglio.
Essi possono anche avere forme ad anello intorno alla base dei petali. La prossima orbitale, ℓ = viene chiamato un f orbitale.
La teoria degli orbitali molecolari tratta gli orbitali come onde e quindi quando si parla di interferenza costruttiva ci si riferisce da due onde se ne forma formazione una che è più alta delle altre due. Qual è la configurazione elettronica dello ione calcio e del floruro () e rappresenta l’ordine di riempimento degli orbitali.
Nel caso della configurazione elettronica di ioni si trova sulla tavola periodica l’elemento neutro e per stabilire il numero di elettroni, se è uno ione positivo si toglierà uno o più elettroni all’elemento, se è negativo si aggiungerà uno o più elettroni. Orbitali molecolari - Teoria Riassunto scolastico che illustra chiaramente la teoria degli orbitali Molecolari e la sua importanza.
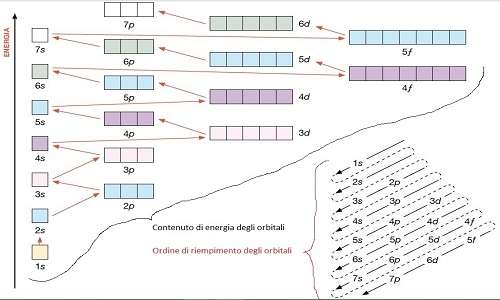
Un orbitale può essere in modo sintetico 1s(1=N, s=forma, 2= numero elettroni) L’ordine di riempimento degli orbitali non segue i livelli energetici, ma le diagonali rappresentate sopra. L’elettrone non ruota attorno al nucleo dell’atomo descrivendo orbite circolari o ellittiche, ma si muove disordinatamente, velocissimo, cambiando continuamente la sua distanza dal nucleo.
In questo suo moto riempie un certo volume che viene chiamato orbitale. Il primo livello energetico ha un solo orbitale di forma circolare detto 1s.
Il quadratino in alto a sinistra è detto diagramma orbitale. Ogni quadratino è un orbitale. Nel primo livello energetico abbiamo un solo orbitale, quello 1s.
Nel secondo livello abbiamo due tipologie di orbitali: s e p. L’orbitale s ha energia più bassa rispetto gli orbitali p, quindi si riempie prima, mentre i tre orbitali p sono degeneri e si trovano a energia leggermente più alta. Ordine in cui gli orbitali sono ordinati secondo energie crescenti, secondo la regola di Madelung. Il termine sp indica il tipo di orbitali atomici puri da cui gli ibridi si sono formati, in questo caso un.
Spedizione GRATUITA sul tuo primo ordine spedito da Amazon. Come gli atomi hanno diversi orbitali atomici (1s, 2s, 2p, etc.), così le molecole possono avere diversi orbitali molecolari.
L’energia di un orbitale molecolare dipende in parte dalla posizione relativa dei nuclei. Il numero di orbitali molecolari formati è uguale al numero di orbitali atomici combinati. Orbitali Molecolari_a. L'energia è la valuta della chimica.
Gli orbitali molecolari sono disposti in ordine di energia crescente. La configurazione da seguire è la seconda, cioè quella di atomi multielettronici.
Solo 17% degli utenti ha risposto correttamente. A causa dell’elevato numero di orbitali atomici combinati (dell’ordine del numero di Avogadro), gli orbitali molecolari che si ottengono sono caratterizzati da livelli energetici molto vicini e costituiscono un quasi continuum, chiamato banda di valenza.
Nessun commento:
Posta un commento
Nota. Solo i membri di questo blog possono postare un commento.